Nessuna malattia colpisce di più di quella cardiovascolare, e, la relazione tra fitness e incidenza di patologie cardiovascolari, è stata oramai confermata da diversi ricercatori. L’esercizio fisico esercita i suoi effetti benefici attraverso diversi meccanismi molecolari, che determinano una regressione dell’aterosclerosi coronarica, apportando diversi benefici come per il miocardio, il sistema cardiovascolare, muscolare, metabolico, sistemi neurali, respiratori e termoregolatori.
L’allenamento aerobico continuato (CET = continuous endurance training) è un tipo di attività fisica che viene eseguita per un periodo di tempo prolungato, con carico di lavoro sub-massimale, sufficiente per aumentare la frequenza cardiaca (HR) e pressione sanguigna. In soggetti con patologie cardiache stabili, 3 sessioni a settimana, con 1 ora di attività, all’intensità del 75-80% della frequenza cardiaca massima, ha migliorato la capacità di lavoro di picco del 21%, dopo 6 settimane. Nell’insufficienza cardiaca, 20 studi hanno dimostrato che l’allenamento CET, è efficace nei pazienti con funzione ventricolare sinistra compromessa, dove si è osservato un miglioramento del 18-34% nella capacità di lavoro di picco (PWC). Linee guida per la prevenzione delle malattie cardiovascolari, incoraggiano nello svolgimento del lavoro aerobico. La Società Europea di Cardiologia, suggerisce intensità da moderate a vigorose con una durata di 30 minuti / sessione a 3-5 giorni / settimana, per un totale di almeno 150 min / sett, mentre l’American College of Sports Medicine e l’American Heart Association sono più precisi e raccomandano attività aerobica almeno 3 giorni / settimana per 20-60 min / sessione più un riscaldamento da 10 a 15 minuti, con un’intensità compresa tra il 40% e l’80% della frequenza di riserva.
Dall’introduzione dell’High Intensity Interval Training (HIIT) di Wisløff et al. nel 2007, diversi studi sono stati eseguiti utilizzando l’HIIT in varie popolazioni cliniche. Negli ultimi anni, diversi studi su soggetti con problematiche cardiovascolari, hanno confermato un miglioramento del VO2 di picco, in seguito a questo lavoro. L’allenamento piramidale, potrebbe essere un’alternativa valida, durante la riabilitazione cardiaca o con la prosecuzione attraverso lavori domiciliari, perché i risultati sono paragonabili al all’allenamento continuato. Pertanto, anche una combinazione dei tre allenamenti, possono essere offerti, in maniera tale da migliorare l’aderenza nel tempo.

L’HIIT sembra essere superiore rispetto agli altri nel migliorare la capacità funzionale. Anche l’allenamento di forza oggi è incluso nel migliorare l’efficienza fisica di soggetti con problematiche cardiovascolari, e, di conseguenza, le società mediche lo raccomandano. Il miglioramento della massa e della forza muscolare, può essere tra il 2% e il 15% in donne e uomini a tutte le età, ed è associato a miglioramento della densità ossea, percentuale di grasso corporeo, risposta dell’insulina all’insulina e pressione sanguigna. Analizzando gli effetti dell’allenamento della forza muscolare in soggetti patologie cardiovascolari, una recente meta-analisi ha concluso che la forza, in combinazione con l’allenamento aerobico, ha aumentato la capacità di esercizio.
CAMBIAMENTI MOLECOLARI INDOTTI DALL’ESERCIZIO FISICO
La perdita della massa muscolare scheletrica contribuisce direttamente all’intolleranza nello svolgimento delle attività quotidiane, il quale è un forte predittore di qualità della vita e mortalità. La perdita muscolare è principalmente guidato dal sistema ubiquitina-proteasoma (UPS), autofagia e segnalazione mediata dalla miostatina.
La miostatina, è un regolatore negativo della massa muscolare, prodotto e rilasciato dai miociti, andando a modulare la crescita e la differenziazione muscolare.
L’autofagia, è un processo in cui proteine mirate sono intrappolate in un autofagosoma, ed è elevato in condizioni di deperimento muscolare, come la denervazione nell’invecchiamento, il digiuno e insufficienza cardiaca. L’esercizio fisico influenza l’UPS, l’autofagia e sistema di miostatina nelle patologie cardiache, in quanto c’è una chiara evidenza che l’esercizio fisico modula l’UPS e il sistema miostatina.
Gielen e colleghi, hanno riferito che, dopo 4 settimane di allenamento aerobico continuo (al 70% VO2 di picco), si è avuto una riduzione dell’espressione di mRNA MuRF-1 del 32,8%, nei soggetti di 55 anni e del 37,0% nei soggetti di età intorno ai 65 anni.
Per quanto riguarda la miostatina, Lenk et al. hanno investigato 24 soggetti con insufficienza cardiaca (stadio NYHA IIIb), e l’allenamento, ha comportato una riduzione del 36% dell’mRNA e una diminuzione del 23% della proteina miostatina rispetto al basale.
Oltre ad un aumento della degradazione proteica, la ridotta sintesi proteica, può anche avere un impatto sulla massa muscolare. Uno dei fattori anabolici più potenti è l’insulina fattore di crescita I (IGF-I), in quanto è un indice dell’alterazione della composizione corporea, della carenza anabolica e dell’attivazione di citochine infiammatorie, in soggetti con insufficienza cardiaca.
Biopsie muscolari da soggetti con disfunzione dell’arteria coronaria stabili, dopo un lavoro di forza, hanno mostrato un aumento dell’IGF-I. Inoltre, in soggetti con insufficienza cardiaca, 6 mesi di esercizio fisico, hanno comportato un aumento dell’81% dell’espressione di IGF-I nel muscolo scheletrico.
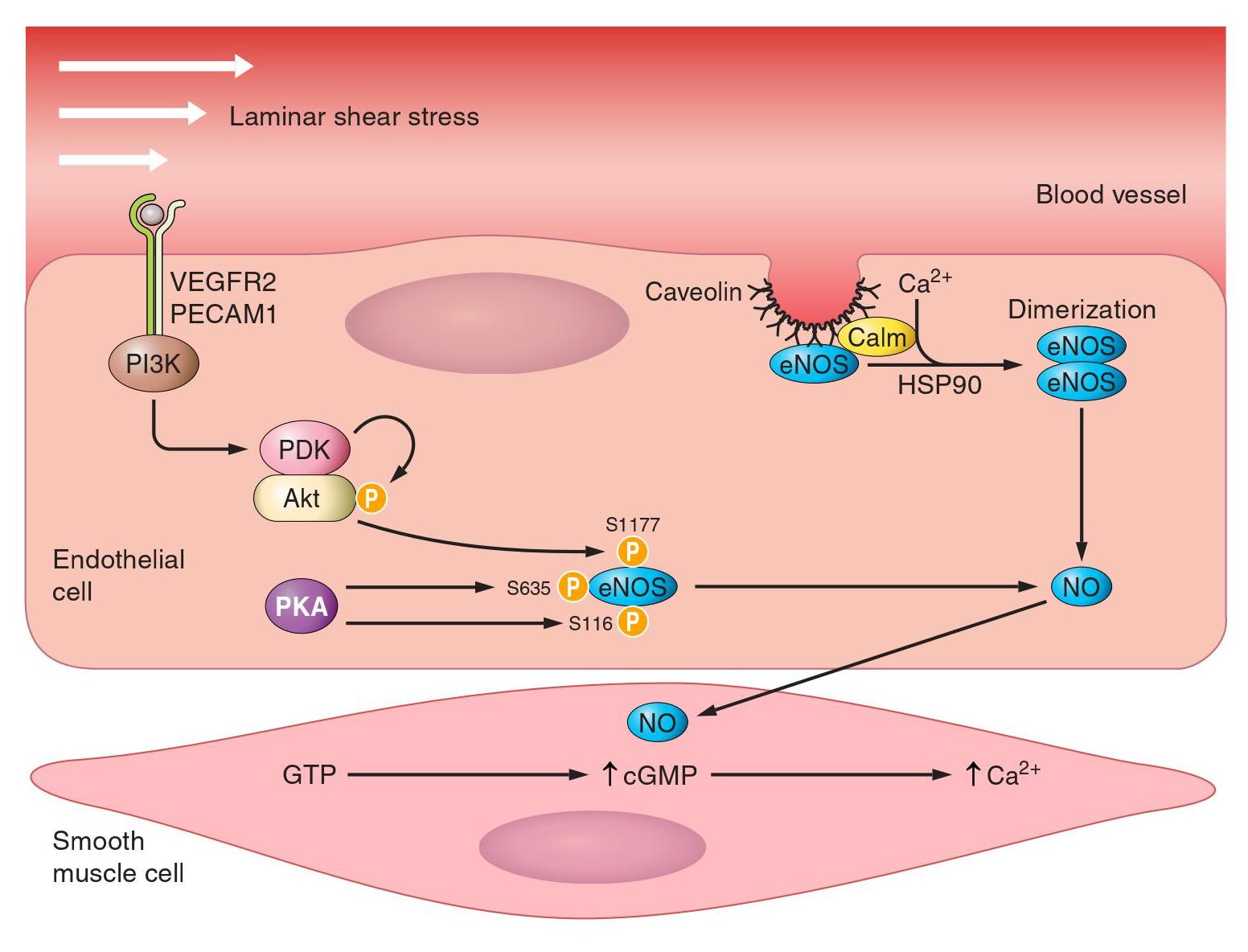
Le proteine miofibrillari sono altamente suscettibili al danno ossidativo e dati recenti hanno fornito prove che l’ossidazione delle proteine sarcomeriche contribuisce alla riduzione della forza (tra cui carbonilazione di lisina, arginina e residui di prolina, nitrazione dei residui di tirosina, ossidazione tiolica e formazione del legame disolfuro). Un aumento dei ROS è giustificato dall’aumento di NAD (P) H ossidasi , xantina ossidasi (XO) e disfunzione mitocondriale attraverso il disaccoppiamento della catena di trasporto degli elettroni e la perdita di elettroni dal complesso I e dal complesso II. L’esercizio fisico ha un impatto sui ROS invertendo questi processi. La rigenerazione di fosfocreatina dall’ATP mitocondriale è essenziale per la contrazione muscolare a lunga durata. Pertanto, il controllo della funzione mitocondriale nelle cellule muscolari scheletriche è fondamentale. Sessioni di esercizio fisico continuato, producono maggiore ATP con una correlazione diretta con l’aumento di VO2 di picco e densità mitocondriale. Oltre agli effetti diretti sui mitocondri, l’esercizio fisico aumenta l’ossido nitrico (NO) nel muscolo scheletrico stimolando l’isoforma dell’ossido nitrico sintasi, che stimola la biogenesi mitocondriale attraverso la proteina-chinasi attivata dall’AMP e una sovra-regolazione del recettore PGC-1a. Per quanto riguarda l’allenamento di forza, si è osservata una diminuita espressione di miR-378, nel vasto laterale, dopo 12 settimane di lavoro. Un cambiamento nel livello di miR-378, è correlato con un guadagno in massa magra.
La dispnea, che limita frequentemente le attività quotidiane dei soggetti con insufficienza cardiaca, è causata dalla disfunzione del diaframma, e negli studi, è stato registrato che la disfunzione di questo muscolo, è una caratteristica nell’insufficienza cardiaca sistolica o diastolica. A livello molecolare, si registra un passaggio di fibre, dal tipo II al tipo I, mentre nella muscolatura periferica, si registra uno spostamento da tipo I a tipo II. Un altro meccanismo potenziale responsabile della riduzione di forza del diaframma, è la carbonilazione di proteine contrattili (principalmente catena pesante di actina e miosina), che va a compromettere così l’efficienza ottimale. L’aumento della carbonilazione e la conseguente perdita di funzione, sono dovuti ad un aumento dei ROS. La carbonilazione di proteine, in particolare, può essere ridotta dall’esercizio fisico, fornendo integrità delle giunzioni neuromuscolari e dell’espressione di recettori nicotinici di Ach. Anche la disfunzione endoteliale è oramai un segno distintivo per lo sviluppo di aterosclerosi, e l’esercizio fisico, può prevenire lo sviluppo di aterosclerosi. È importante ricordare che l’insorgenza della disfunzione endoteliale, è un forte predittore per eventi cardiovascolari futuri. Un programma di esercizio aerobico continuato di 4 settimane, è efficace nell’attenuare la vasocostrizione arteriosa nel condotto epicardico anche del 54%, con un aumento della velocità di picco del flusso medio sanguigno del 78%, tutto confermato da diversi studi in pazienti con disfunzione della coronaria o diabete.
ESERCIZIO FISICO E ATTIVAZIONE DELL’OSSIDO NITRICO SINTASI ENDOTELIALE
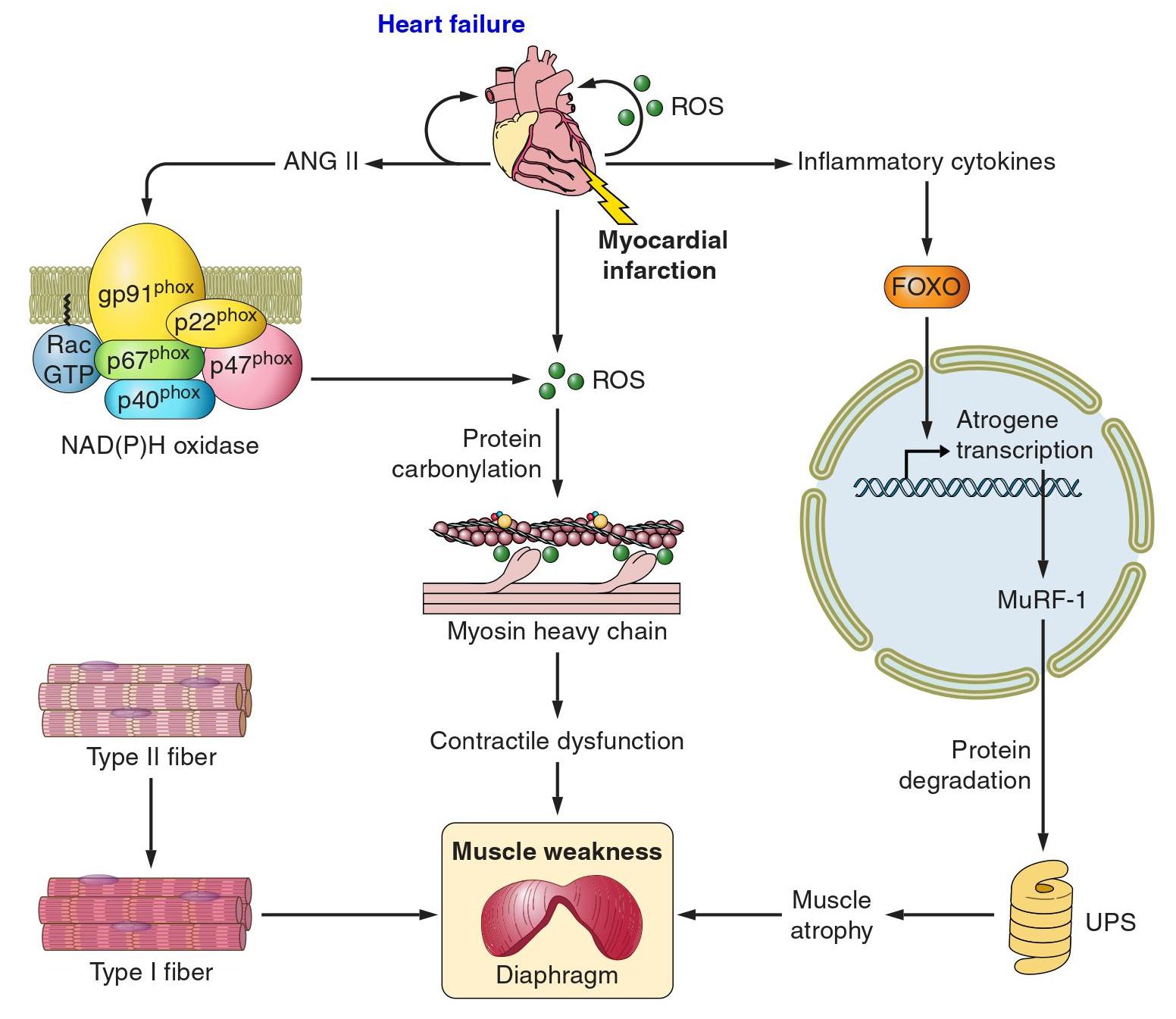
La produzione di ossido nitrico (NO), il principale fattore di regolazione della vasodilatazione, è mediato dall’ossido nitrico sintasi endoteliale (eNOS). L’attivazione di eNOS si basa su un’attivazione a più fasi. Il primo passo è l’attivazione è Ca2+ dipendente. L’entrata di Ca2+ nella cellula e la sua interazione con la calmodulina, innesca il rilascio di eNOS dalle membrane plasmatiche, dove è collegato e inattivo. In un secondo momento, l’eNOS si associa con proteine da shock termico (Hsp90), portando così alla dimerizzazione dell’enzima che produce l’osido nitrico. All’aumentare dello stress da taglio nei vasi, in seguito all’esercizio fisico, la cascata di segnalazione viene avviata dall’attivazione di recettori meccanici, come il recettore VEGF2 o molecola di adesione delle cellule endoteliali piastriniche 1 (PECAM1), seguito dalla fosfatidilinositolo 3-chinasi (PI3K). Un altro percorso di attivazione di eNOS mediato dallo stress da taglio, avviene tramite integrine, le quali collegano la matrice extracellulare con la rete di actina. Le integrine interagiscono con diverse molecole coinvolte nella segnalazione, come ad esempio l’adesione focale chinasi (FAK).
ESERCIZIO FISICO E STRESS OSSIDATIVO
La biodisponibilità di ossido nitrico non dipende solo dalla generazione di eNOS, ma è anche influenzato dai ROS. La bassa biodisponibilità di NO è in parte causata dalla reazione di specie reattive all’ossigeno (ROS) con ossido nitrico (perossinitrito). Un altro enzima che genera ROS nel sistema vascolare, è il sistema eNOS stesso. In alcune condizioni patologiche, la riduzione enzimatica dell’ossigeno molecolare mediante eNOS, non è più accoppiato all’ossidazione dell’arginina L, con conseguente produzione di ROS. Il disaccoppiamento dell’ossido nitrico sintasi, è stato implicato in diverse patologie tra cui l’aterosclerosi, diabete e insufficienza cardiaca. Un fattore critico per questo disaccoppiamento, è la biodisponibilità del tetraidrobiopterina (BH4), un cofattore per la reazione enzimatica. Fattori genetici possono portare alla diminuzione della velocità nella biosintesi di BH4, determinando riduzioni sostanziali sia nel plasma che nel sistema vascolare, dei livelli di BH4. Questo è stato associato ad aumentati livelli di ROS e una ridotta vasorilassazione ad Ach.
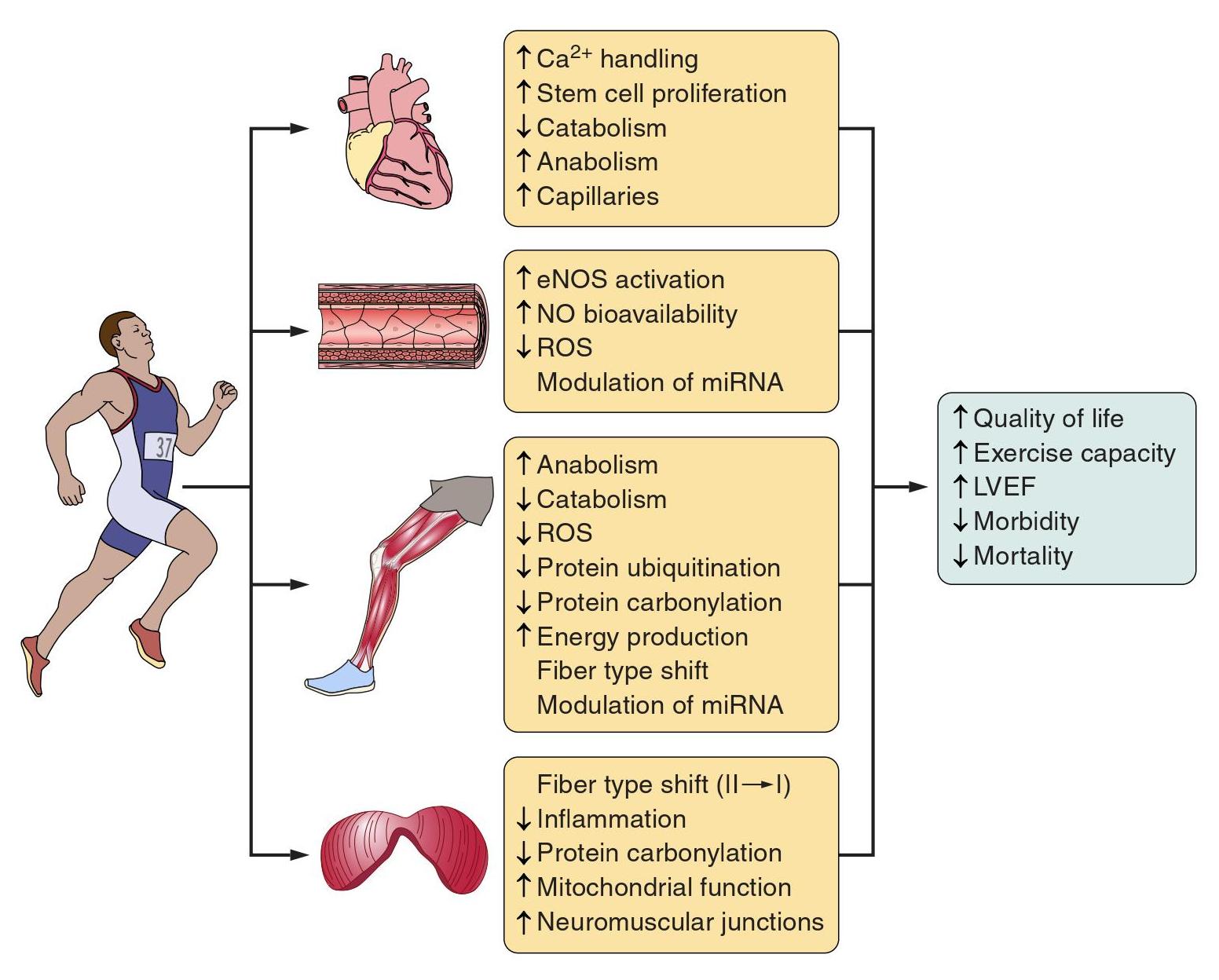
Rimane il fatto che, in una meta-analisi recentemente pubblicata, che include 15 randomizzati studi controllati condotti su 813 soggetti, hanno concluso che l’allenamento aerobico continuo, inverte il rimodellamento ventricolare sinistro e migliora la frazione di eiezione ventricolare sinistra (LVEF), volume telediastolico e volume sistolico terminale. Oltre agli effetti noti dell’esercizio sul sistema neuro-ormonale, sono importanti anche altri 3 meccanismi: la modulazione del sistema catabolico / anabolico, alterazioni nella gestione del Ca2+, e la modulazione della proliferazione delle cellule staminali. Durante gli ultimi anni, si è arrivati a comprendere alcuni cambiamenti molecolari, responsabili dell’intolleranza all’esercizio in soggetti con insufficienza cardiaca, ed è evidente che l’esercizio fisico, apporta il suo effetto benefico in un modo multifattoriale.
BIBLIOGRAFIA
Volker Adams, Bernhard Reich, Madlen Uhlemann and Josef Niebauer “Molecular effects of exercise training in patients with cardiovascular disease: focus on skeletal muscle, endothelium, and myocardium” Am J Physiol Heart Circ Physiol 313: H72–H88, 2017.

